| 发现之旅 |  |

我们知道胶体分为固溶胶、液溶胶和气溶胶。而雾、云、烟等都属于气溶胶,在早晨的树林中,由于有很多的小水滴分散在空气中,使空气形成一种气溶胶,从而在阳光的照射下形成一道道光柱。而在中午,树林中的水都蒸发完了,空气变的很干燥,不再是胶体,所以光柱消失了。
在化学实验室里也可以看到类似的现象,用手电筒的光来照射一杯溶液和一杯胶体:

| 深入思考 |  |
一、布朗运动
1827年,英国植物学家布朗把花粉悬浮在水中,用显微镜可以观察到小颗粒在做不停的、无秩序的运动,这种现象叫做布朗运动。
用超显微镜观察胶体,也可以发现胶体粒子在做布朗运动。
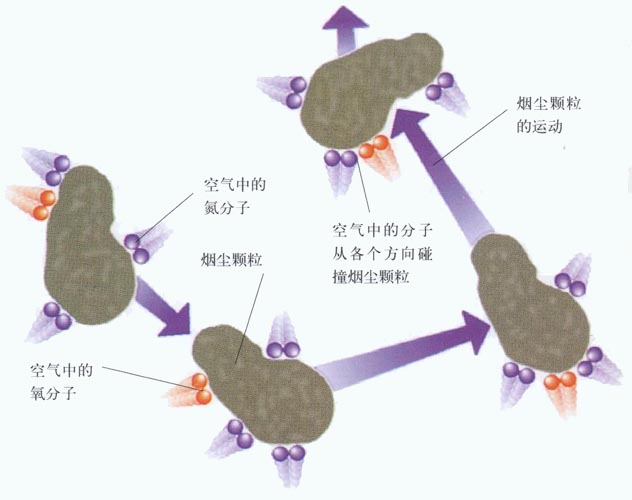
烟尘的布朗运动
在盛有红褐色Fe(OH)3胶体的U形管的两个管口分别插入一个电极,通入直流电:
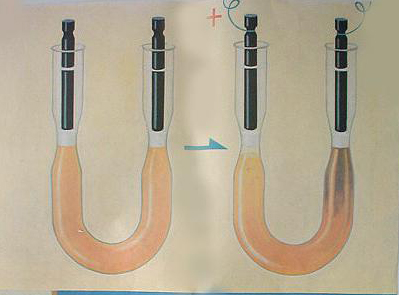
电泳现象
像这种在外加电场作用下,胶体粒子在分散剂里向电极定向移动的现象叫做电泳。
医学上利用血清的纸上电泳来进行某些疾病的诊断。电泳在生物化学和电镀上也有很广泛的用途。
三、凝聚
有些胶体凝聚后,胶体的微粒和分散剂凝聚在一起成为不流动的冻状物,叫做凝胶。例如:豆腐就是把盐卤(MgCl2・6H2O)或石膏(CaSO4・2H2O)溶液加入豆浆里,使豆浆里的蛋白质和水等一起凝聚,形成凝胶。

豆腐的制作
把混有离子或分子杂质的胶体装入半透膜的袋子里,并置袋于溶剂中,从而使离子或分子从胶体溶液里分离的操作,叫做渗析。
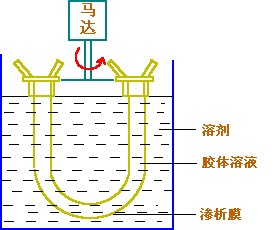
渗析
| 学有所用 |  |
1.给Fe(OH)3胶体和淀粉胶体通直流电,有何区别?
因此,Fe(OH)3胶体电泳,由于Fe(OH)3胶粒带正电,故阴极区颜色加深,而淀粉胶粒由于不带电,故没有明显现象。
| 沙场练兵 |  |
1. 关于胶体和溶液的区别,下列叙述中正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中的溶质微粒不带电,胶体中分散质微粒带有电荷
C.通电后,溶液中溶质微粒分别向两极移动,胶体中分散质微粒向某一极移动
D.溶液与胶体的本质区别在于分散质微粒直径大小,前者小于1nm,后者介于1nm~100nm
2. 下列关于Fe(OH)3胶体的说法不正确的是 ( )
A.Fe(OH)3溶胶与硅酸溶胶混合将产生凝聚现象
B.Fe(OH)3胶体在电场作用下;向阳极运动
C.Fe(OH)3胶体微粒不停地作布朗运动
D.光线通过Fe(OH)3溶胶时会发生丁达尔现象
3. 下列事实与胶体的性质有关的是( )
①用盐卤点豆腐 ②用明矾净水 ③医药上用三氯化铁止血 ④江河入海口形成三角洲
A.只有①② B.只有①②④
C.只有①②③ D.全部
4. 用半透膜把分子或离子从胶体溶液中分离出来的方法叫( )
A.电泳
B.电解
C.凝聚 D.渗析
5. 向氢氧化铁溶胶中逐渐加入一种液体,先使溶胶发生凝聚而沉淀,继续加入该液体又使沉淀溶解。这种液体是( )
A.KOH溶液
B.氨水
C.稀盐酸 D.NH4Cl溶液
6. 将某溶液逐滴加入Fe(OH)3溶胶内,开始时产生沉淀,继续滴加时沉淀又溶解,该溶液是 ( )
A.2mol/LH2SO4溶液
B.2mol/LNaOH溶液
C.2mol/LMgSO4溶液
D.硅酸溶胶
7. 有一胶体溶液,在电泳时它的胶体微粒向阳极移动;将这胶体溶液分别加入下列物质①蔗糖②硫化钠③硅酸胶体④氢氧化铁胶体,不发生凝聚的是( )
A.①和② B.②和③ C.①和③ D.①和④
