| 发现之旅 |  |
我国清代文学家蒲松龄所写的短篇小说《聊斋志异》里,常常谈到“鬼火”。旧社会里迷信的人,还把“鬼火”添枝加叶地说成是什么阎罗王出现的鬼灯笼。那么,“鬼火”究竟是怎么回事呢?

不管白天还是黑夜,都有磷化氢冒出,只不过白天日光很强,看不见“鬼火”罢了。为什么夏天的夜晚在墓地里常看到“鬼火”,而“鬼火”还会“走动”呢?夏天的温度高,易达到磷化氢气体着火点而出现“鬼火”,又由于燃烧的磷化氢随风飘动,所以所见的“鬼火”还会走动。大家以后看到鬼火就不会觉得惊讶和害怕了吧!
| 深入思考 |  |
磷原子的最外层有五个电子,与氮元素同属于第ⅤA族。在下图中显示了磷原子的外层电子结构:

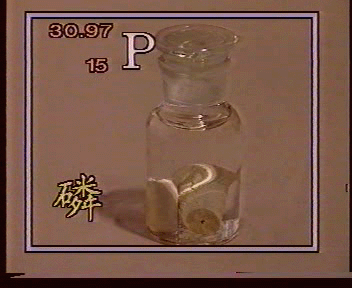
白磷

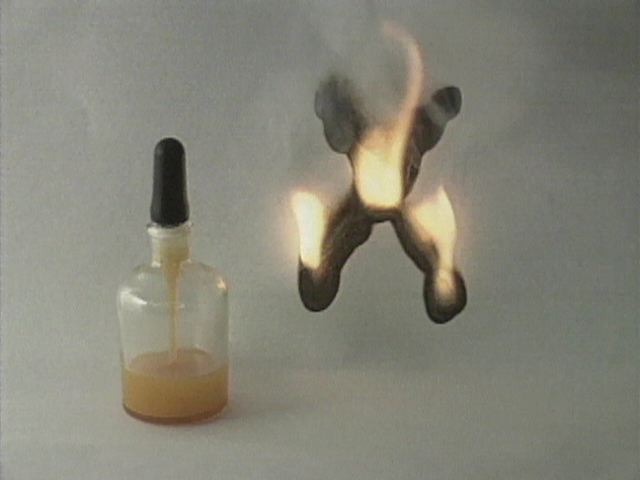
白磷自燃
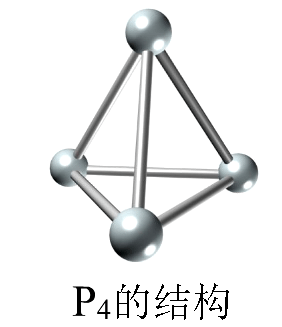
磷在氧气中点燃则生成五氧化二磷。

磷广泛存在于动植物组织中,并与蛋白质或脂肪结合成核蛋白、磷蛋白和磷脂等,也有少量其它有机磷和无机磷化合物。除植酸形式的磷不能被机体充分吸收和利用外,其它大都能为机体利用。 在自然界中,磷以磷酸盐的形式存在,是生命体的重要元素。存在于细胞、蛋白质、骨骼和牙齿中。
| 学有所用 |  |
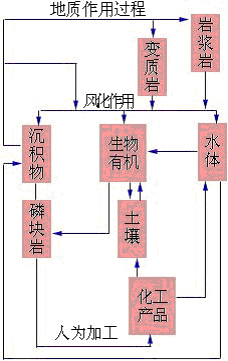
磷灰石构成了磷的巨大储备库,而含磷灰石岩石的风化,又将大量磷酸盐转交给了陆地上的生态系统。与水循环同时发生的则是大量磷酸盐被淋洗并被带入海洋。在海洋中,它们使近海岸水中的磷含量增加,并供给浮游生物及其消费者的需要。而后,进入食物链的磷将随该食物链上死亡的生物尸体沉入海洋深处,其中一部分将沉积在不深的泥沙中,而且还将被海洋生态系统重新取回利用。埋藏于深处沉积岩中的磷酸盐,其中有很大一部分将凝结成磷酸盐结核,保存在深水之中。一些磷酸盐还可能与 SiO2 凝结在一起而转变成硅藻的结皮沉积层,这些沉积层组成了巨大的磷酸盐矿床。通过海鸟和人类的捕捞活动可使一部分磷返回陆地。但从数量上比起来,每年从岩层中溶解出来的以及从肥料中淋洗出来的磷酸盐要少多了。其余部分则将被埋存于深处的沉积物内。
| 沙场练兵 |  |
1. 已知下列事实:①硝酸的酸性比磷酸强;②硝酸显强氧化性,磷酸不显强氧化性;③氮气与氢气可直接化合,磷与氢气很难直接化合;④氨比磷化氢稳定.其中能说明氮的非金属性比磷元素强的是( )
A.①②③ B.①②④ C.①③④ D.①②③④
2. 关于非金属元素N、O、Cl、P的叙述,正确的是
( )
A.在通常情况下其单质均为气体
B.其单质均由双原子分子构成
C.都属于主族元素
D.每种元素仅生成一种氢化物
3. 关于磷的下列叙述中,正确的是( )
①红磷没有毒性而白磷剧毒 ②白磷在空气中加热到260 ℃可转化为红磷 ③少量白磷保存于水中 ④红磷可升华,且转化为白磷时属化学变化
⑤白磷和红磷都可溶于CS2⑥白磷为非金属单质,其晶体为正四面体型的原子晶体
A. ①②③ B. ②③④
C. ①③④ D. ③⑤⑥
4.
下列关于磷及其化合物的叙述不正确的是
( )
A. 红磷用于制造安全火柴和农药
B. 磷酸二氢盐都易溶于水
C. 磷酸是三元酸,比硝酸的酸性强
D. 五氧化二磷溶于热水生成磷酸,溶于冷水生成偏磷酸
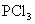 ,
,
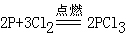
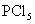 ,
,
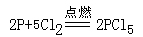
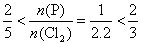 ,故产物是
,故产物是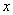 ,氯气的物质的量为
,氯气的物质的量为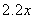 。
。
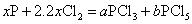
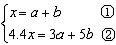
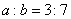
 为
为 为
为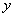 ,则
,则